الألدهيدات: هيكل ، خواص ، تسمية ، استخدامات وأمثلة
الألدهيدات عبارة عن مركبات عضوية لها الصيغة العامة RCHO. يمثل R سلسلة أليفاتية أو عطرية ؛ C إلى الكربون ؛ أو الأكسجين و H إلى الهيدروجين. وهي تتميز بوجود مجموعة من الكربونات وكذلك الكيتونات والأحماض الكربوكسيلية ، بحيث يطلق على الألدهيدات أيضًا مركبات الكاربونيل.
تعطي مجموعة الكاربونيل الألدهيد العديد من خصائصه. إنها مركبات تتأكسد بسهولة وتتفاعل بشدة مع الإضافات النووية. تحتوي الرابطة المزدوجة لمجموعة الكاربونيل (C = O) على ذرتين لها اختلافات في شحنتهما للإلكترونات (الكهربية).
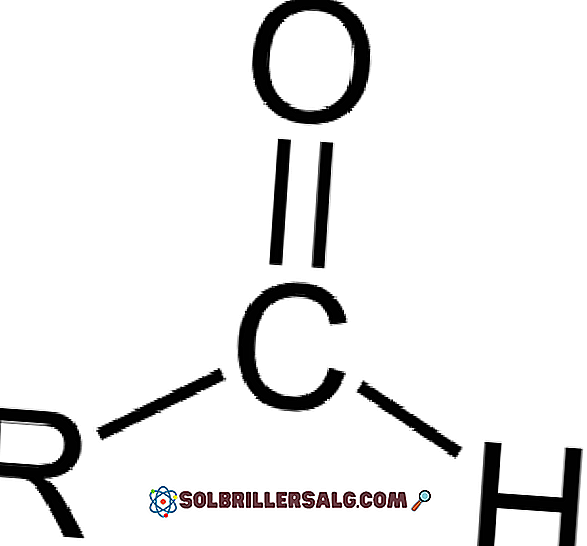
يجذب الأكسجين الإلكترونات بقوة أكبر من الكربون ، لذلك تتحرك السحابة الإلكترونية نحوه مما يجعل الرابطة المزدوجة بين الكربون والقطب الأكسجين ، مع لحظة ثنائي القطب مهمة. وهذا يجعل المركبات الألدهيدات القطبية.
سوف تؤثر قطبية الألدهيدات على خواصها الفيزيائية. تكون نقطة الغليان وقابلية الألدهيدات في الماء أكبر من المركبات الكيميائية غير القطبية ذات الأوزان الجزيئية المماثلة ، مثل حالة الهيدروكربونات.
الألدهيدات التي تحتوي على أقل من خمس ذرات كربون قابلة للذوبان في الماء ، لأن روابط الهيدروجين تتشكل بين أكسجين مجموعة الكربونيل وجزيء الماء. ومع ذلك ، فإن زيادة عدد الكربون في سلسلة الهيدروكربونات يؤدي إلى زيادة في الجزء غير القطبي من الألدهيد ، مما يجعله أقل قابلية للذوبان في الماء.
لكن كيف حالهم ومن أين أتوا؟ على الرغم من أن طبيعتها تعتمد بشكل أساسي على مجموعة الكاربونيل ، فإن بقية التركيب الجزيئي تسهم أيضًا في الكل. وبالتالي ، يمكن أن تكون من أي حجم ، صغيرة أو كبيرة ، أو حتى جزيء كبير يمكن أن يحتوي على مناطق تسود فيها طبيعة الألدهيدات.
وهكذا ، كما هو الحال مع جميع المركبات الكيميائية ، هناك الألدهيدات "اللطيفة" والأخرى المريرة. يمكن العثور عليها في المصادر الطبيعية أو توليفها على نطاقات كبيرة. أمثلة على الألدهيدات هي الفانيلين ، الموجود للغاية في الآيس كريم (الصورة العليا) والأسيتالديهيد ، مما يضيف نكهة إلى المشروبات الكحولية.
التركيب الكيميائي

تتكون الألدهيدات من كاربونيل (C = O) ترتبط به ذرة الهيدروجين مباشرة. هذا يميزه عن المركبات العضوية الأخرى مثل الكيتونات (R 2 C = O) والأحماض الكربوكسيلية (RCOOH).
يظهر التركيب الجزيئي حول - CHO ، مجموعة فورميل في الصورة العليا. مجموعة فورميل مسطحة لأن الكربون والأكسجين لهما تهجين sp2. هذا الكوكب يجعله عرضة للهجوم من الأنواع النووية ، وبالتالي يتأكسد بسهولة.
ماذا يشير هذا الأكسدة؟ لتشكيل رابطة مع أي ذرة أخرى أكثر الكترونيا من الكربون ؛ وبالنسبة للألدهيدات فهو أكسجين. وبالتالي ، يتأكسد الألدهيد إلى حمض الكربوكسيل ، - COOH. ماذا لو تم تقليل الألدهيد؟ الكحول الأولي ، ROH ، سيتم تشكيله في مكانه.
يتم إنتاج الألدهيدات فقط من الكحوليات الأولية: تلك التي تكون فيها مجموعة OH في نهاية السلسلة. بشكل مشابه ، تكون مجموعة formyl دائمًا في نهاية السلسلة أو تبرز منها أو الحلقة كعنصر بديل (إذا كان هناك مجموعات أخرى أكثر أهمية ، مثل -COOH).
الخصائص الفيزيائية والكيميائية
كونها مركبات قطبية ، فإن نقاط انصهارها أعلى من تلك الموجودة في المركبات غير القطبية. لا تستطيع جزيئات الألدهيد الارتباط الجزيئي من خلال روابط الهيدروجين ، لأنها تحتوي فقط على ذرات كربون مرتبطة بذرات الهيدروجين.
بسبب ما سبق ، فإن الألدهيدات لديها نقاط غليان أقل من الكحوليات وأحماض الكربوكسيل.
ذوبان النقاط
الفورمالديهايد -92 ؛ أسيتالديهايد -121 ؛ بروبيونالديهايد -81 ؛ n- بوتيرالدهيد -99 ؛ ن-فاليرالديهايد -91 ؛ Caproaldehyde - ؛ heptaldehyde - 42؛ فينيل أسيتالديهيد -؛ بنزالديهايد -26.
نقاط الغليان
الفورمالديهايد -21 ؛ أسيتالديهايد 20 ؛ بروبونالديهايد 49 ؛ ن بوتيرالدهيد 76 ؛ ن-فاليرالديهايد 103 ؛ Caproaldehyde 131؛ Heptaldehyde 155؛ فينيل أسيتالديهيد 194؛ Benzaldehyde 178
القابلية للذوبان في الماء معبراً عنها في غرام / 100 غرام من H 2 O
الفورمالديهايد ، قابل للذوبان للغاية. أسيتالديهيد ، لانهائي ؛ بروبيونالديهايد ، 16 ؛ ن بوتيرالدهيد ، 7 ؛ ن فاليرديهايد ، قابل للذوبان بشكل طفيف ؛ caproaldehyde ، قابل للذوبان قليلا. قليل الذوبان فينيل أسيتالديهيد ؛ Benzaldehyde ، 0.3.
تميل نقاط الغليان للألدهيدات إلى الزيادة مباشرة مع الوزن الجزيئي. على العكس من ذلك ، هناك ميل إلى تقليل قابلية الذوبان للألدهيدات في الماء مع زيادة وزنها الجزيئي. وينعكس هذا في الثوابت الفيزيائية للألدهيدات المذكورة أعلاه.
التفاعلية
تفاعل الأكسدة
يمكن أكسدة الألدهيدات إلى حمض الكربوكسيل المناظر في وجود أي من هذه المركبات: Ag (NH 3 ) 2 ، KMnO 4 أو K 2 Cr 2 O 7 .
التخفيض إلى المشروبات الكحولية
يمكن هدرجة هذه المواد بمساعدة محفزات النيكل أو البلاتين أو البلاديوم. وبالتالي ، يتم تحويل C = O إلى C-OH.
التخفيض إلى الهيدروكربونات
في وجود Zn (Hg) ، حمض الهيدروكلوريك المركز أو في NH 2 NH 2 ، تفقد الألدهيدات مجموعة الكربونيل وتصبح هيدروكربونات.
إضافة النواة
هناك العديد من المركبات التي تمت إضافتها إلى مجموعة الكاربونيل ، من بينها: الكواشف Grignard ، السيانيد ، ومشتقات الأمونيا والكحول.
تسمية
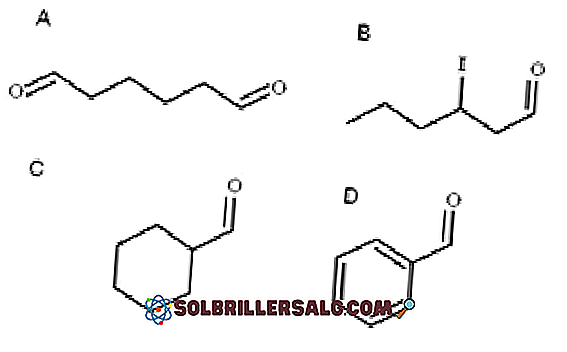
في الصورة العليا أربعة ألدهيدات موضحة. كيف يتم تسمية؟
بالنظر إلى أنها كحول أولي مؤكسد ، يتم تغيير اسم الكحول إلى -ol---by. وهكذا ، يسمى الميثانول (CH 3 OH) إذا تم أكسده إلى CH 3 CHO الميثانال (الفورمالديهايد) ؛ CH 3 CH 2 CHO ethanal (أسيتالديهيد) ؛ CH 3 CH 2 CH 2 CHO propanal و CH 3 CH 2 CH 2 CH 2 CHO butanal.
جميع الألدهيدات المسماة حديثًا لها مجموعة CHO في نهاية السلسلة. عندما يكون في كلا الطرفين ، كما في A ، في النهاية ، تتم إضافة البادئة di-. نظرًا لأن A يحتوي على ستة كاربونات (تحسب كلاً من مجموعتي formyl) ، فهو مشتق من هكسانول واحد ، وبالتالي يكون اسمه: قرص الهكسان.
عندما يكون هناك بديل ، مثل جذري ألكيل ، أو رابطة مزدوجة أو ثلاثية ، أو هالوجين ، يتم سرد كربون السلسلة الرئيسية مع إعطاء رقم CHO 1. وبالتالي ، يسمى الألدهيد B: 3-iodohexanal.
ومع ذلك ، في الألدهيدات C و D ، لا تتمتع مجموعة CHO بالأولوية لتحديد المركبات المذكورة من الآخرين. C هو سيكلوكلان ، بينما D a بنزين ، وكلاهما يستبدل بـ H من مجموعة فورميل.
في نفوسهم ، حيث أن الهيكل الرئيسي هو دوري ، تسمى مجموعة فورميل الكاربالديهايد. وهكذا ، C هو cyclohexanecarbaldehyde ، و D هو benzenecarbaldehyde (المعروف باسم benzaldehyde).
تطبيقات
هناك الألدهيدات في الطبيعة قادرة على منح النكهات اللطيفة ، مثل حالة سينامالديهايد ، المسؤولة عن النكهة المميزة للقرفة. هذا هو السبب في كثير من الأحيان أنها تستخدم النكهات الاصطناعية في العديد من المنتجات مثل الحلويات أو الطعام.
الفورمالديهايد
والفورمالديهايد هو الألدهيد الذي يتم إنتاجه صناعيًا بكمية أكبر. يستخدم الفورمالديهايد الناتج عن أكسدة الميثانول في محلول 37 ٪ من الغاز في الماء ، تحت اسم الفورمالين. يستخدم هذا في دباغة الجلود وفي حفظ وتحنيط الجثث.
وبالمثل ، يستخدم الفورمالديهايد كمبيد للجراثيم ومبيدات الفطريات ومبيدات الحشرات للنباتات والخضروات. ومع ذلك ، فائدتها الكبرى هي المساهمة في إنتاج المواد البوليمرية. يتم تصنيع البلاستيك الذي يطلق عليه الباكليت بواسطة التفاعل بين الفورمالديهايد والفينول.
الباكليت
Bakelite عبارة عن بوليمر لهيكل ثلاثي الأبعاد ذو صلابة كبيرة يستخدم في العديد من الأدوات المنزلية مثل الأواني اليدوية والمقالي وآلات صنع القهوة والسكاكين وما إلى ذلك.
مصنوعة البوليمرات المماثلة للباكليت من الفورمالديهايد مع مركبات اليوريا والميلامين. لا تستخدم هذه البوليمرات كدائن فحسب ، بل تُستخدم أيضًا كمادة لاصقة ومواد طلاء.
خشب رقائقي
الخشب الرقائقي هو الاسم التجاري للمادة المكونة من صفائح رقيقة من الخشب ، والتي انضم إليها البوليمرات المنتجة من الفورمالديهايد. يتم تصنيع العلامات التجارية فورميكا وميلماك بمشاركة هذه العلامة. فورميكا هي مادة بلاستيكية تستخدم في تغطية الأثاث.
يستخدم Melmac البلاستيك في إعداد الأطباق والنظارات والأكواب ، إلخ. والفورمالديهايد هو مادة خام لتوليف مركب الميثيلين-ثنائي فينيل-ديزوسيانات (MDI) ، سلائف البولي يوريثان.
البولي يوريثين
يتم استخدام مادة البولي يوريثين كعزل في الثلاجات والمجمدات ، وحشو الأثاث ، والمراتب ، والطلاءات ، والمواد اللاصقة ، والنعال ، إلخ.
butyraldehyde
بوتيرالدهيد هو مقدمة رئيسية لتوليف إيثيل هكسانول 2 ، والذي يستخدم كملدّن. يحتوي على رائحة تفاح لطيفة تسمح باستخدامه في الأطعمة كنكهة.
كما أنها تستخدم لإنتاج المعجلات المطاطية. يتدخل باعتباره كاشف وسيط في صناعة المذيبات.
الأسيتالديهيد
تم استخدام الأسيتالديهيد في إنتاج حمض الخليك. لكن وظيفة الأسيتالديهايد هذه انخفضت أهميتها ، حيث تم استبدالها بعملية الكربنيل الميثانول.
تركيب
الألدهيدات الأخرى هي سلائف كحول أوكسو ، والتي تستخدم في إنتاج المنظفات. يتم تحضير ما يسمى كحوليات الأكسجين عن طريق إضافة أول أكسيد الكربون والهيدروجين إلى الأوليفين للحصول على الألدهيد. وأخيراً يتم مهدرجة الألدهيد للحصول على الكحول.
تستخدم بعض الألدهيدات في صناعة العطور ، كما هو الحال في شانيل رقم 5. العديد من الألدهيدات ذات الأصل الطبيعي لها رائحة لطيفة ، على سبيل المثال: heptanal لها رائحة العشب الأخضر ؛ الأوكتان رائحة برتقالية. و nonanal رائحة الورود والسترال رائحة الجير.
أمثلة على الألدهيدات
غلوتارالدهيد
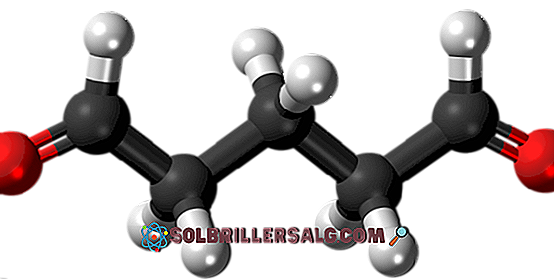
يحتوي glutaraldehyde في بنيته مجموعتين formyl في كلا الطرفين.
يتم تسويقه تحت اسم Cidex أو Glutaral ، ويستخدم كمطهر لتعقيم الأدوات الجراحية. يتم استخدامه في علاج الثآليل على القدمين ، وتطبيق نفسه كسائل. كما أنه يستخدم كعامل تثبيتي الأنسجة في مختبرات الأنسجة وعلم الأمراض.
بنزيلديهايد
إنه أبسط الألدهيد العطري الذي يتكون من حلقة بنزين حيث ترتبط مجموعة فورميل.
يوجد في زيت اللوز ، وبالتالي فإن رائحته المميزة تسمح باستخدامه كنكهة غذائية. بالإضافة إلى ذلك ، يتم استخدامه في تخليق المركبات العضوية المتعلقة بتصنيع الأدوية وفي صناعة البلاستيك.
غليسيرألدهيد
وهو ألدوتريوز ، سكر مكون من ثلاث ذرات كربون. يحتوي على اثنين من الأيزومرات التي تدعى enantiomers D و L. glyceraldehyde هو أول أحادي السكاريد الذي يتم الحصول عليه في عملية التمثيل الضوئي خلال المرحلة المظلمة (دورة Calvin).
غليسيرألدهيد-3-فوسفات

ويتضح هيكل glyceraldehyde-3-الفوسفات في الصورة العليا. تتوافق الكرات الحمراء بجانب الأصفر مع مجموعة الفوسفات ، في حين أن الكرات السوداء تماثل الهيكل العظمي الكربوني. الكرة الحمراء المرتبطة بالأبيض هي مجموعة OH ، ولكن عندما تكون مرتبطة بالكرة السوداء والأخيرة بالكرة البيضاء ، فهي مجموعة CHO.
غليكيرالديهايد - 3 - الفوسفات تشارك في تحلل ، وهي عملية التمثيل الغذائي التي يتحلل فيها الجلوكوز إلى حمض البيروفيك مع إنتاج ATP ، خزان الطاقة من الكائنات الحية. بالإضافة إلى ذلك ، من إنتاج NADH ، وهو عامل الحد البيولوجي.
في تحلل الغليسيات ينشأ فوسفات غليسيرالديهايد 3 - فوسفات ثنائي هيدرو أسيتون من انقسام D- الفركتوز -1-6-فوسفات
يتدخل glyceraldehyde-3-phosphate في عملية التمثيل الغذائي المعروفة باسم دورة البنتوز. في هذا ، يتم إنشاء NADPH ، مخفض بيولوجي مهم.
11-رابطة الدول المستقلة الشبكية
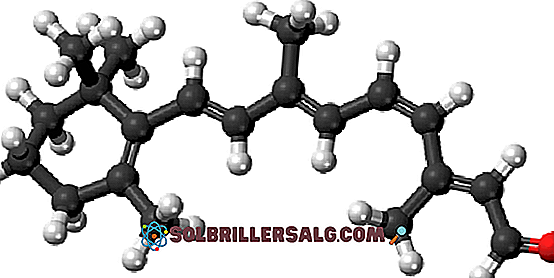
car كاروتين هو صبغة طبيعية موجودة في العديد من الخضروات ، وخاصة في الجزر. وهو يعاني من تمزق مؤكسد في الكبد ، يتحول إلى ريتينول كحول أو فيتامين أ. أكسدة فيتامين (أ) وما يترتب عليه من إيزومرة لاحقة من روابطه المزدوجة تشكل الألدهيد 11-رابطة الدول المستقلة.
فوسفات البيريدوكسال (فيتامين ب 6)
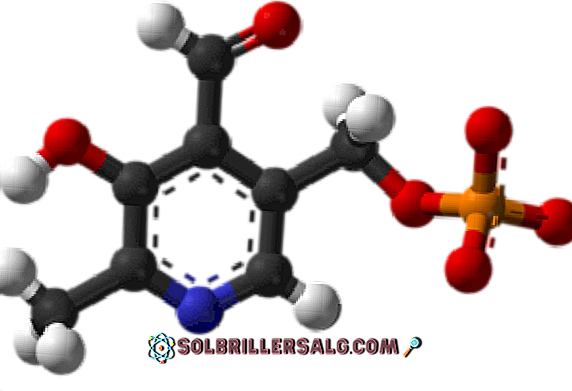
إنها مجموعة اصطناعية مرتبطة بالعديد من الإنزيمات ، وهي الشكل النشط لفيتامين B6 وتشارك في عملية التخليق للناقل العصبي المثبط GABA.
أين هي مجموعة formyl في هيكلها؟ لاحظ أن هذا يختلف عن بقية المجموعات المرتبطة بالحلقة العطرية.
ساليسيلالدهيد
وهو مادة خام لتوليف حمض الصفصاف ، وهو دواء مسكن وخافض للحرارة يعرف باسم الأسبرين.







